Nouvelles demandes

Soumettre une nouvelle demande
Pour obtenir un certificat de conformité aux monographies de la Pharmacopée Européenne (CEP), les demandeurs doivent envoyer les documents suivants, au format électronique, au Service de la Certification des substances (DCEP) de l’EDQM...

Contenu du dossier
Les documents énumérés ci-après donnent des informations détaillées sur ce que doit contenir chaque demande. Reportez-vous au document correspondant à votre situation.
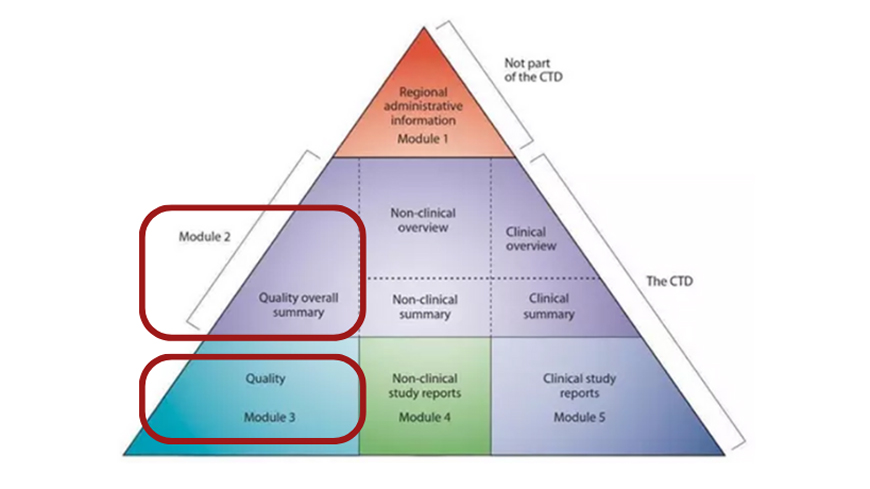
Résumé global de la qualité (QOS) pour les demandes de CEP
Le résumé global de la qualité (QOS) joue un rôle crucial dans la procédure de certification de conformité aux monographies de la Pharmacopée Européenne.

Les dix déficiences principales observées dans les nouvelles demandes de CEP concernant la pureté chimique
Les dix déficiences principales identifiées après l’évaluation initiale des nouvelles demandes de certificats de conformité aux monographies de la Pharmacopée Européenne (CEP) concernant la pureté chimique.
Téléchargez l'infographie (en anglais)

Dossiers frères
La procédure du « dossier frère » a pour but de faciliter la soumission de dossiers similaires dans le cadre de la procédure de Certification, et de permettre aux demandeurs de bénéficier d’une procédure accélérée ainsi que d’évaluations harmonisées.

Format des soumissions et soumission électronique
Les demandeurs doivent envoyer leurs documents au format électronique uniquement au Service de la Certification des Substances (DCEP) de l’EDQM.
- Procédure de Certification : confiance réglementaire et évaluation accélérée
- Quelques astuces pour améliorer la qualité de votre dossier et accélérer l’évaluation de votre demande de CEP
- Top Ten Deficiencies in New Applications for Certificates of Suitability for Chemical Purity PA/PH/CEP (24) 10 (en anglais)
- New requirements for the content of the CEP dossier for chemical purity and for herbal drugs/herbal drug preparations according to the CEP 2.0 (en anglais)
- Titulaires de CEP : comment éviter le rejet d’une notification
- Changement de coordonnées pour une demande de certificats de conformité (à utiliser à partir du 1er avril 2022)
- Responsabilités des titulaires d'un certificat de conformité envers leurs clients (PA/PH/CEP (21) 57, janvier 2022)
Rendez-vous sur la page Documents et lignes directrices Certification pour une liste de tous les guidelines.
La base de données Certification (mise à jour quotidiennement) vous permet de rechercher une liste des CEP accordés, leur type, le nom de la substance, le numéro complet du CEP, la date d'émission et l'état de validité.
Les demandeurs s'engagent à fournir les échantillons de la substance et/ou les impuretés demandées par l'EDQM.




